Specifikus és nem-specifikus immunitás
A test egy nem-specifikus (veleszületett) immunválasz védelmet. amely kiegészül a specifikus (szerzett) immunvédelmet, amely lehetővé teszi ellenállni a baktériumok, vírusok, gombák, paraziták és az idegen makromolekulák. Védelmi funkciók egy organizmus aktus révén antigén, azaz. E. szerek, amelyek stimulálják a specifikus immunrendszer aktiválásával antigén-specifikus T-limfociták (T-sejtek), és a B-limfociták (B-sejtek). B-limfociták differenciálódnak plazma sejtek (plazmasejtek), szekretáló antigénspecifikus ellenanyagot (immunglobulinok, lg) (B). Ig semlegesített és opszonizáló antigének és aktiválja a komplement rendszert. Ezek a mechanizmusok biztosítják a különleges elismerése, a megfelelő antigén és annak későbbi eltávolítása nem specifikus. Néhány T- és B-sejtek immunológiai memóriát.
limfociták antigén nélkül receptor prekurzorok alávetni előfeldolgozás a csecsemőmirigyben (T) és a csontvelő (B). Ezek a szervek termelnek monospecifikus 108 T vagy B-sejtek, amelyek mindegyike ellen irányul a specifikus antigénhez. Naiv T és B sejtek, amelyek még nem találkozott antigént, a testben keringő (perifériás vér nyirok → → nyirokszövet → vérben) és mennek keresztül klonális expanzió és kiválasztási való érintkezés után a specifikus antigén (általában a nyirokszövetekben). Ezután a sejtek elkezdenek gyorsan osztódni, termelő számos monospecifikus leánysejtekbe. Utódsejtjei plazma sejtek (plazmasejtek), vagy a „felfegyverzett” T sejtek, amelyek kezdeményezi a megsemmisítése a antigénnel.
Klonális deléció - egy mechanizmust a megsemmisítése limfocita-receptorokhoz irányított a saját szövetei ellen. Miután a kezdeti kapcsolatot a antigénnel autospetsifichnym ezen limfociták során a fejlesztés korai szakaszában elpusztul a csecsemőmirigy vagy a csontvelőben. Klonális deléció vezet központi immunológiai toleranciát. Az, hogy az immunrendszer megkülönböztetni endogén és az idegen antigéneket úgynevezett elismerése, „ő-idegen”. Ez a képesség alakul szinte azonnal a születés. Minden anyagot felmerült ezúttal a test kell tekinteni endogén ( „saját”), mások azonosították a külföldi ( „idegen”).
Képtelenség megkülönböztetni endogén és exogén komponensek nyilvánul autoimmun betegségek.
Eleinte érintkezik a vírussal (azaz például, kanyaróvírus) nem-specifikus immun mechanizmusok általában nem akadályozza a vírus szaporodását és fejlődését a kanyaró. Specifikus immunrendszer annak T-killer (B2) és lg (első IgM, majd IgG; EOI) lassan reagál megy primer immunválasz, vagy érzékenységet. Aktiválása után az immunrendszer működésének kórokozó elpusztul, t. E. személyt visszanyeri a kanyaró. Szekunder immunválasz vagy érzékenységet: másodlagos fertőzés a specifikus IgG termelt sokkal gyorsabb. A vírus elpusztul gyorsan, és a betegség a második alkalommal nem alakul ki. Ez a fajta védelem a fertőző betegségek elleni nevezzük immunitást. Ő lehet elérni oltás egy speciális antigén (aktív immunizálás). Passzív immunizálás végezhető bevezetésével kész-Ig (immun szérum).
A nem-specifikus immunitás [idézet]
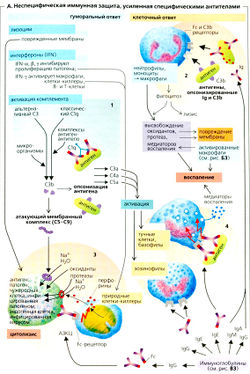
A. Nem-specifikus immun védelmet, megerősített specifikus antitestek
A lizozim és a komplement faktorok jelen a plazmában (A1), valamint a „természetes” killer (NK-sejtek) és a fagociták, különösen a neutrofilek és makrofágok, amelyek a monocitákból származó, hogy a szövetbe vándoroljanak (A2), fontos szerepet játszanak a veleszületett immunitás. A szervezetben keringő neutrofilek, monociták és eozinofil. Ezek kemokin receptorok (például, CXCR1 és 2 az IL-8) és biztosítani, amelyek különböző kemokinek (például IL-8), hogy ezeket a helyeket, ahol a baktériumok behatolnak (kemotaxis). Ezek a sejtek képesek migrálni. Ezek rögzítve az endothelium (marginatsiya) alkalmazásával szelektinek, behatolnak az endotélium (diapedézist), elnyelik és sérülés mikroorganizmusok lizozim felhasználásával oxidáló szerekkel (például H2O2), az oxigén gyökök (O2, OH *, és a nitrogén (N0) oxidot. Erre kell hasítási (lízis) alkalmazásával mikroorganizmus enzimek lizoszómákban. Ha az antigén túl nagy a hasítási (parazita féreg és a t. d.), ezek a sejtek is ekzotsitiruyutsya más szerek részt vesznek nem specifikus immunitás (például proteázokat vagy citotoxikus proteineket ).
Csökkentése enzimek, mint a kataláz és a szuperoxid-diszmutáz, oxidálószer koncentrációja általában megmarad alacsony szinten. Ez az állapot gyakran sérülnek, különösen a makrofág aktiváció (lásd. Az alábbiakban és BZ), hogy teljes mértékben kihasználja a baktericid hatás oxidánsok. Van azonban a gyulladás (A2,4) károsítja a résztvevő sejtek nemspecifikus védelmet, és néhány esetben még más sejtek.
Opszonizáció (A1, 2) van a kötődése opszoninok például IgG és komplement faktor C3b, domének specifikus antigénnel, ezáltal fokozott fagocitózist. Ez az egyetlen módja annak, hogy a baktériumok fagocitálására poliszacharid shell. A fagociták van felszínén lévő receptorokhoz (antigennezavisimogo) IgG-Fc-szegmens és a C3b. Így antigensvyazannye C3b és IgG kötődnek a megfelelő receptorokhoz, és ezáltal összekötő nemspecifikus fagocitózis folyamat specifikus immun védelmi rendszer. Szénhidrát-kötő fehérjék (lektinek) plazma - collectins (például, mannóz fehérje), amelyek rögzített a sejtfalak mikrobák, is jár, mint opszoninok nemspecifikus.
Komplement kaszkád aktiválódik antigének opsonizovannymi Ig (klasszikus úton) és neopsonofilnymi antigének (alternatív útvonal) (A1). Komplement komponensek NWA, C4a és C5a aktiválja bazofil és eozinofil fehérvérsejtek (A4). Komplement komponensek C5-C9 membrannoatakuyuschy generálni komplex (MAC), hogy a defekt és öl (Gram-negatív) baktériumokat citolízis (AZ). Ez a védelem segít formában lizozim (Muramidáz =), egy olyan enzimet, amely elpusztítja a baktériumok sejtfalának, murein tartalmazó. Ez akkor fordul elő granulociták, plazma, nyirok, és a váladék.
A „természetes” killer-sejtek (NK) - nagy granuláris limfociták, szakosodott nem-specifikus védelem a vírusok, mikobaktériumok, tumorsejtek, stb Ezek felismerik a fertőzött és a tumorsejtek „idegen felület” és a biztosított annak az Fc-receptorok .. IgG-opszonizált a felületi antigének (antitest-függő sejt-toxicitási, ADCC, aZ). Perforins, zkzotsitiruemye „természetes” killer-sejtek, pórusok kialakítására a falak, a célsejtek, ami megkönnyíti azok további lízis (citolízist). Ez nemcsak hogy megakadályozza a proliferációt a kórokozó (enzim eszköz sejtek), de lehetővé teszi azt is (és egyéb intracelluláris patogének) egyéb védekező mechanizmusokat a támadás objektumot.
Különböző interferonok (IFN) aktivitását serkentik "természetes" killer-sejtek: IFN-a, IFN-β, és kisebb mértékben, az IFN-y. IFN-a és IFN-β megjelent elsősorban leukociták által és fibroblasztok, mivel az IFN-y szállítjuk az aktivált T-sejtek és a „természetes” killer-sejtek. Vírusfertőzött sejtek kap nagy mennyiségű interferont, aminek következtében megnő vírus fertőzött sejteket vírusok. Defensinek - citotoxikus peptideket felszabaduló fagocitákkal. Lehet, hogy a nem specifikus citotoxikus hatása kórokozók, amelyek rezisztensek a „természetes” killer sejteket (például, a képződése ioncsatornák a membránok a célsejtek).
A makrofágok monocitákból származó, hogy a szövetbe vándoroljanak. Néhány makrofágok szabadon mozgatható (szabad makrofágok), míg a másik (rögzített makrofágok) által határolt régiót, mint például megtalálható a máj sinus (Kupffer-sejtek), pulmonális alveolusok, serosa bél sinus lép, nyirokcsomók, a bőr (Langerhans-sejtek), az ízületi folyadék (szinoviális A-sejtek), az agy (mikroglia) vagy endothelium (így például a vese glomerulusok). mononukleáris fagocita rendszer lor angol. MPS) - egy általános kifejezés a monociták a vérben keringő, makrofágok és a keringő a szövetekben. A makrofágok felismerik viszonylag nem-specifikus szénhidrát komponensek felvitele a baktériumok, és elnyelik azokat fagocitózissal. Aktiválódnak abban az esetben, kórokozók túlélni a fagoszómájában (cm. Alul és BR).
Specifikus immunitás: sejt-közvetített immunválasz [szerkesztés]
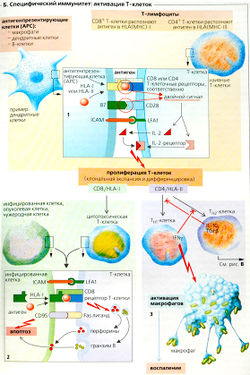
B. specifikus immunitás: aktiválása a T-sejtek
Mivel egy specifikus sejt-közvetített immunválasz a „felfegyverzett” effektor T-sejtek aktiválást igényel a néhány nap, ez az úgynevezett késleltetett típusú immunválasz. Ez bevonását igényli speciális antigén-prezentáló sejtek (APC): a dendritikus sejtek, makrofágok és B-sejtek. APC-kezelt sejtek és a jelen antigén peptideket a T-sejtekhez kapcsolódó MHC-1 és az MHC-ll fehérjéket, ezáltal egy jel adására kostimuláció aktiválásához szükséges a naiv T-sejtek. (Az ezen fehérjéket kódoló gének a fő hisztokompatibilitási komplex (MHC) I (MHC-1) és a II (MHC-II) osztályokba; HLA [humán leukocita antigén) - elfogadott megnevezése MHC férfi) fertőzött dendritikus sejtek (lokalizálódik. főleg Nyirokszövet) általában úgy viselkednek, mint az APC. Az ilyen HLA-függő antigén prezentáció (B1) tartalmazza a találmány egy antigén HLA kötőhely. ICAM [angol, intracelluláris adhéziós molekula) felszínén APC ezután társított LFA-1 (1 antigént, a limfocita funkció) a membrán a T-sejtek. Amikor a T-sejtek antigénre specifikus komplexet képez kötést fokozódik, és a kettős jelzés ARS elősegíti aktiválását és klonális szelekciója a T-sejtek (B1).
APG kettős jelzés áll: 1) az antigén felismerését (HLA-függő antigén I vagy II osztály) T-sejt-receptorok és ko-receptorok, és 2) a csont-mulyatornogo jelet, azaz kötő fehérje 67 (az APC) protein .. CD28 a T-sejtek (B1). CD8 molekula a citotoxikus T-sejtek (T-sejt-= T-killer sejt), és a CD4-molekula a T-helper sejtek (Th-sejt) függvény, mint társ-receptorok. Ha az antigénkötő nélkül fordul elő ko-stimuláció (például a májban, ahol nincs APC), B-limfociták inaktivált, azaz. E. Legyen erőteljes, és fejleszti a perifériás immuntoleranciát.
T-sejtek képesek fogadni kettős jelzés ARS fertőzött makrofágok vagy B-sejtek, amely lehetővé teszi kötődését azok receptoraihoz, hogy az antigén (például, rovar- vagy kígyóméreg, vagy egy allergén). Kettős APC jel vált T-sejtek szekretálnak interleukin-2 (IL-2), és megkötik a megfelelő receptor interleukin-2 (B1). IL-2 egy valós jelet az ilyen monospecifikus klonális expanziója T-sejtek. Dolgozik a autokrin és parakrin mechanizmusokat.
A IL-2 inhibitorok, például a ciklosporin A, hatékony immunszuppressziót lehet elérni, például a szervátültetés.
A klonális expanzióját a T-sejtek differenciálódnak három "felfegyverzett" altípus r. E. A citotoxikus T-sejtek (T-sejtek vagy T-killer sejtek) és a T-helper I. típusú (Th1-sejtek) és a II típusú (Th2 sejtek). Ezek a sejtek nem kell egy kifejezett egy kostimuláció és más típusú adhéziós molekulák (VLA-4 helyett az L-szelektin), amelyen keresztül már rögzítésre a gyulladt szöveti endotéliumon (inkább, mint a nyirokszövetekben ahogy elődeik képzetlen].
T-killer sejtek fejlődnek ki, naiv tartalmazó CD8 (CD8 +) T-sejtek után HLA-l-függő antigén prezentáció (B2). Endogén antigénprezentáció akkor jelentkezik, amikor a fehérje elnyeli HLA-I antigén (kórokozó citoszolt fehérje) a citoszol APC, mint általában a helyzet. A T-sejt-receptor, a CD8-asszociált protein, egy gyilkos T-sejt felismerésére képes HLA-I - korlátozott antigének fertőzött (vírus) endogén sejtekben a tumorsejteken, és a sejtek a transzplantált szervek. Ez következetesen vezet sejt apoptózis (programozott sejthalál), vagy nekrózis. Összekapcsolása Fas-ligandum CD95 (= Fas) vezet ugyanaz, mint a proteáz granzyme B, hogy belép a sejtbe a pórusokon keresztül kialakított abszorbeált (exocitozissal) perforin (B2).
Amikor egy HLA-ll-dependens bemutatása (B1) antigén intracelluláris vezikulumokat (például abszorbeált (fagocitózissal) baktériumokkal vagy virális burokfehérjék, azaz. E. Egy exogén antigén prezentáció), a naiv CD4 + T-sejteket transzformáljuk éretlen T-helper (7 / ud), amely differenciálódnak Th1 vagy T-sejtek. TH1 sejtek által indukált gyulladásos válasz és elősegítik makrofág aktiváció alkalmazásával IFN-y (BZ), míg a Th2-sejtek esszenciálisak aktiváló B-sejtek (B2). Th1 és Th2 sejtek elnyomják egymást, úgy, hogy csak az egyik típusú sejtek a két érvényesül a sejt-közvetített immunválasz (BR).
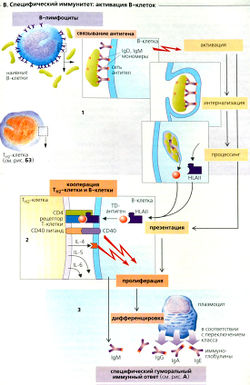
A specifikus immunitás: B-sejtek aktiválását
Specifikus immunitás: humorális immunválaszt [szerkesztés]
Humorális immunitás - függvénye a B-sejtek (B1). Számos monomer IgD és IgM, csatlakozik a B-sejtek felületén, kötődnek a megfelelő antigént (IgM oldatban pentamerjeként). A kapott hálózati antigensvyazannyh LG vezet internalizáció (felszívódás) és feldolgozott antigén-antitest komplex a B-sejtek. Azonban, a B-sejt-aktiválást igényel egy második jelet, amely lehet szállított közvetlen útvonal thimic-független (TI, angol, independ) antigént (pl bakteriális poliszacharid), vagy közvetve - a TH2 kpetok ha tímusz-függő (TD, angol, függenek) antigén . Az utóbbi esetben, a B-sejtek továbbítja HLA-ll-korlátozott antigén TD TH2-sejtek (B2). Amikor C04-asszociált T-sejt-receptor (TCR) TH2-sejtek felismerik az antigént a felületén TH2 sejtek expresszált CD40-ligandum (CD40 ligandok kötődnek a CD40 fehérjék felszínén B-sejtek) és a szekretált IL-4. CD40-ligandum és IL-4 (a továbbiakban IL-5 és IL-6) stimulálják a klonális kiválasztása B-sejtek, a váladék a IgM és differenciálódásukhoz plazmasejtek (EOI). lg class switching bekövetkezte előtt differenciálódás, t. e. alternatív splicing a DNS expresszálható különböző típusú nehéz láncok LG. Ezért, IgM alakítjuk IgA, IgG vagy IgE. Minden típus LG, származó klón B-sejtek, monospecifi- ugyanahhoz az antigénhez. Plazma kialakult sejtek váltás után osztályok, amelyek kizárólag egyféle immunglobulin.