kovalens kötés
A módszer a vegyértékkötéseket a következők:
1. A kovalens kötés van kialakítva két elektron ellentétes forog, ahol az elektron pár tartozik két atom.
2. A kovalens kötés az erősebb, annál az átfedő elektron felhők.
Kovalens kötés - típusú kémiai kötés. keresztül végrehajtott a kialakulását egy elektronpár, amely tartozik mindkét atom. Kijelölt „:” vagy „-”.
A mechanizmus a kovalens kötés van osztva:
- csere kovalens kötés;
- donor-akceptor kovalens kötés.
Az Exchange kovalens kötés fordul elő, a szénatomok közötti. Amennyiben minden egyes atom ad egy párosítatlan elektront a teljes elektronpár.
Donor-akceptor jelentése egy kovalens kötés, amely egy atom (donor) ad egy elektronpár, és a többi atom (akceptor) előírja a pár szabad orbitális.
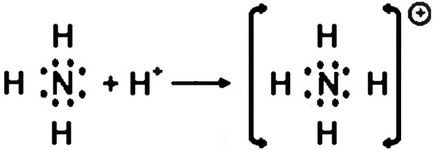
Amellett, hogy egyszeres kötéseket, képezhetnek kettős és hármas kovalens kötés.
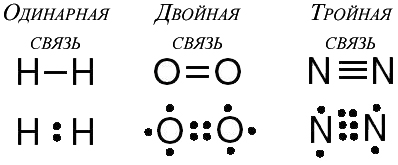
Tulajdonságok A kovalens kötés.
- telítettség
- orientáció;
- polarizálhatóságot.
Telítettség - képes alkotni szigorúan bizonyos mennyiségű kovalens kötések (1-től 6), amely meghatározza a maximális lehetséges vegyértékű elem.
Irányítottság - aspirációs atomokkal a legnagyobb elektronsűrűség között a magok.
A polarizálhatóságának - elmozdulása elektronok hatása alatt egy külső elektromos mező.
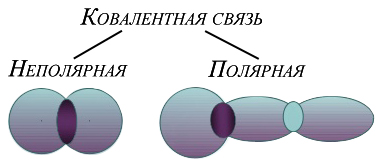
- apoláros kovalens kötés, amely elektron felhő által alkotott közös elektronpárt elosztott térben képest szimmetrikusan a magok a két atom (példák: Cl2, N2).
- poláris kovalens kötés, azaz a teljes elektron felhő smesh felé az egyik atom, úgy, hogy van aszimmetria töltés eloszlásának (példák: CO, H2O).
Elektronegativitás - az a képesség, hogy késleltesse az atomokkal maga teljes elektronpár.