ATP szintézis
ATP (adenozin-trifoszfát) molekula, élő sejtek energiát biztosít [szabály]
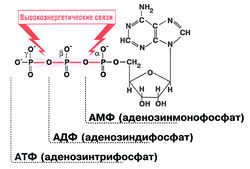
Ábra. 10.1. A szerkezet az adenozin-trifoszfát (ATP)
ATP molekulák létfontosságúak. ATP energiaforrás szükséges az izom-összehúzódást, ingerület vezető, szivárgás számos biokémiai reakciók, stb Nyugalmi elfogyasztott 28 g (1 uncia) ATP percenként, egyenértékű 1,4 kg (3 font) per óra, és terhelésre ATP fogyasztás eléri a 0,5 kg percenkénti! ATP áll adenin, ribóz és a három-foszfát csoportok úgynevezett a-, β- és y-foszfát-csoportok (ábra. 10.1). Hidrolízise magas fosfoangidridnyh β- közötti kötések foszfor atomok között vagy az A- és β-foszfor atom kibocsátások szükséges energia a biokémiai reakciók, azaz a hogy fenntartsák az élet a szervezet.
A legtöbb energetikailag kedvező módszer az ATP szintézis - ez az aerob oxidatív foszforiláció. Azonban, az ATP is kialakíthatók anaerob körülmények között. bár kisebb hatékonysággal. Háromféle módon anaerob szintézisét ATP: szubsztrát foszforiláció, a ATP képződése és foszfokreatin kapott adenilatkinaznoy reakciót. Bár anaerob szintézise ATP-t és nem energetikailag kedvező, a képesség, hogy szintetizálni ATP hiányában oxigén létfontosságú lehet.
A szintézisét ATP szubsztrát foszforiláció [idézet]
Ábra. 10.2 azt mutatja, hogy az ATP képződik a glikolízis során, és közben fosfoglitseratkinaznoy piruvatkinaznoy reakciók és a Krebs-ciklus során a reakció enzim katalizálja szukcinil-CoA szintetáz bevonásával nukleozidtsifosfatkinazy (ábra. 10.3). Megjegyzés: ezek a reakciók oxigén nem szükséges.
Ábra. 10.2. A ATP képződése révén glikolízis során szubsztrát foszforiláció
Ábra. 10.3. A Krebs-ciklus van kialakítva szubsztrát foszforiláció GTP, amelyet azután hatására nukleozid-difoszfát kináz ATP
Előállítása ATP foszfokreatin [idézet]
Foszfokreatin - a „sürgősségi ellátás” nagy energiájú foszfát, amelyet fel lehet használni a gyors kialakulását ATP szükséges az izom-összehúzódást anaerob körülmények között. Ez az intenzív ATP szintézis mechanizmus vészhelyzetekben az életmentés; azonban phosphocreatine tartalékok töltött nagyon gyorsan, mindössze néhány másodperc.
A nyugalmi időszakok, amikor sok ATP, kreatin-kináz foszforilezi kreatin alkotnak phosphocreatine. Különösen fontos szerepe van ennek a reakciónak az izmokban. Ha azt szeretnénk, hogy egy hirtelen, éles rántással phosphocreatine foszforilálja ADP: ATP szükséges az izom-összehúzódás (ábra. 10.4) Emiatt is nevezik phosphocreatine „phosphogen”.
Ábra. 10.4. A formáció ATP foszfokreatin terhelés alatt és foszfokreatin kreatin szintézise a pihenőidő
A kreatin kimeneti formájában kreatinin [idézet]
Kreatin - jelentése egy aminosav. nem része a fehérje. A kreatin szintetizálódik arginint és a vizelettel ürül formájában kreatinin. Vér kreatinin, kreatinin clearance becsléséhez használt glomeruláris filtrációs ráta, károsodott vese- munkát. Megjegyzés: Ne keverd össze a kreatin, a kreatinin és a karnitin.
Kreatin javítja a teljesítményt [idézet]
Teljesítménynövelő szerek - olyan anyagok, amelyek növelik a sebességet, erőt és kitartást sportoló. Sokan közülük veszélyes és tilos használni. A vélemények ellentmondásosak, azonban sok tudós egyetért abban, hogy a kreatin - csak teljesítménynövelő szer, amely tudományosan bizonyított, hogy növelje a hatékonyságot az ingatlanok, mint a sprint, és folyamatos nyomás alatt.
A ATP képződése származó ADP hatására adenilát [idézet]
Miután ATP hidrolizált energia kibocsátása céljából szükséges az izom-összehúzódást, a sejtekben termelődött és halmozódott ADP. Azonban, ADP is tartalmaz energiaigényes és fosfoangidridnuyu-kötés (ábra. 10.1). Nature találmány: ez az energia válik hozzáférhetővé, miután anaerob két molekula ADP adenilát-kináz alatt ATP formájában (10.5 ábra.) (Korábbi néven enzim adenilát miokinazoy).
Ábra. 10.5. A kialakulásának két molekula ATP ADP a reakcióban adenilatkinaznoy
Aerob ATP szintézis [idézet]
ATP szintézis a légzési lánc oxidatív foszforiláció [idézet]
A mitokondriumok [idézet]
Ábra. 11.1. diagramja a szerkezet a mitokondriumok
Mitokondrium - organellumokból hasonló méretű a bakteriális sejt. Érdemes megjegyezni, hogy a mitokondriumok két membrán. A külső membrán porin átitatott molekulák. Porins csatornákat képeznek, amelyeken keresztül át tud hatolni a membránon, molekulatömege kisebb, mint 10 kDa. A belső membrán lényegében átjárhatatlan; képez süllyesztékekbe - Kristen. Az egész belső membrán szabadon át csak kis molekulák - mint például a H2 0 és NH3. Kevés más molekulák segítségével a hordozó proteinek és gyűjtő rendszerek képesek leküzdeni ezt az akadályt.
Úgy véljük, hogy a mitokondrium - egy példa endosymbiosis. A belső membrán A mitokondriumok a fogoly az ő tartalmát egykor egy ősi anaerob baktérium, amely behatolt primitív sejtek korai szakaszában az evolúció. Fennmaradt nyomait a múlt: például, a mitokondriumok saját DNS (mtDNS), kódoló gének 37. 24 közülük részt vesznek a broadcast mtDNS fehérjéket kódolnak más légzési lánc. Figyelemre méltó, csak a 13 ki az összes fehérje a mitokondriális légzési lánc (összesen 85) vannak kódolva mtDNS. A másik kódol a nukleáris DNS, és azok szállítása a mitokondrium a citoszolba.
Légzési lánc [idézet]
Ábra. 11.2. elektron transzport a légzési láncban. A diagram azt mutatja, az elektronok áramlását, a közbenső metabolit a Krebs-ciklus (malát és szukcinát), hogy az oxigén a elektrontranszfer lánc komplexek révén az I, II, III, IV
Légzési lánc - hatékony módja a termelő ATP-t és NADH-t használva FADN2 során képződött oxidációs anyagcsere „tüzelőanyag” [főként szénhidrátok és a zsírsavak]. A légzési lánc áll, öt komplexek - I, II, III, IV, és egy komplex gomba alakú (komplex V). Gomba „multicomplex” áll alegységek F1 (alegység „egy”) és F0 (alegység „O” összeköti oligomicinnel). Néhány a légzési lánc komplexek tartalmaznak citokrómok, amely közlekedési az elektronok a lánc: citokróm III komplexen tartalmaz b, és komplex IV - citokróm / DS. Továbbá, az elektrontranszport részt ubikinon (Q10 koenzim), és citokróm C Minden légzési lánc komplexek található a belső mitokondrium-hártyán. Komplexek I, III és IV nemcsak elektrontranszport hanem funkcionálhat molekuláris proton szivattyúk: ők „pumpált” protonok a mátrixból a intermembrán helyet. A belső membrán impermeábilis, különösen, hogy nem ereszti át a protonok, így azok újra a mátrix csak egy módon - át a proton csatorna komplex F1 / F0, amely ezen a ponton szintetizálja ATP.
Az elektronok áramlását, leegyszerűsítve ábrán látható.
mitokondriális patológia [idézet]
Vannak különféle rendellenességeinek a légzési lánc. Sokan közülük genetikailag keresztül továbbítják az anyai vonal, mint az összes mitokondrium zigóta jön a mitokondriumok a tojás. Az osztódó sejtekben ezer mtDNS molekulák véletlenszerűen vannak elosztva a utódsejtek, azonban a különböző szövetek tartalmazhat mind normál, mind a mutáns mtDNS-molekula (ezt az állapotot nevezik heteroplazmia). Következésképpen a klinikai képet ilyen kórképek igen változékony. Mutációk nukleáris gének kódoló légzési lánc fehérjéket, autoszomális típusú, és általában okoz súlyosabb betegségek.
Leber-féie látóideg-sorvadás [idézet]
Leber látóideg-sorvadás okozza a mutáció helye a mitokondriális DNS-t, amely kódolja az egyik alegységet komplex I. Ebből megsérti a mitokondriális légzési lánc szenved legfőképpen, úgy tűnik, a látóideget. A betegség felnőttkorban okoz látásvesztés.
Mitokondriális encephalomyopathiákban tejsavas acidózist és a stroke-epizódok (MELAS-szindróma) [szabály]
Ennek oka az, MELAS-szindróma - mtDNS génben mutációt kódoló leucin transzfer RNS mitokondriumok. Ez a mutáció befolyásolja a fordítást a mtDNS, és ezért a MELAS-szindróma megzavarta a szerkezet a légzési lánc komplexek kivéve Complex II, amely teljes mértékben által kódolt nukleáris genomjába.
Leigh-kór [szerkesztés]
Leigh-betegség - a degeneratív betegség a központi idegrendszer jellemző kóros elváltozásokat. Általában alakul korán. A betegség genetikailag heterogén: leggyakrabban az oka a betegség mutációs helyek a nukleáris genom kódoló komponenseket a légzési lánc, de néhány esetben, hogy a betegség alakul mutációk miatt a mitokondriális gének. Amikor Li betegség lehet megzavarta aktivitását ATP szintáz (komplex V) vagy komplexek I, II, III, IV. Egyes formája a betegség Lee azok megsértették a tevékenység a piruvát-dehidrogenáz komplex.
Piruvát-dehidrogenáz komplex deficiencia növekedéséhez vezet a vérben koncentrációja piruvát, laktát és alanin. Egyes betegeknél megfigyelt javulást, ha figyelembe liponsav és a tiamin (koenzim a piruvát-dehidrogenáz komplex). Korlátozott sikerrel ketogén terápia vonatkozik az alacsony szénhidráttartalmú diéta. (Ketontestek könnyen át a vér-agy gáton, és azok katabolizmus képződött acetil-CoA függetlenül piruvatdegirogenaznogo komplex.)
Bioszintézise ATP oxidatív foszforiláció (I. rész) [szabály]
Bioszintézise ATP a légzési lánc, amely részt vesz, mint egy patak elektronok (e-) és fluxus protonok (H +) fordul elő oxidatív foszforiláció. A légzési lánc négy komplexek (I, II, III, IV), és a gomba alakú szerkezet - ATP-szintáz-alegység F0 / F1 vagy komplex V, amely szintetizálja az ATP ADP és szervetlen foszfát (Pi). Alatta lesz szó, hogyan lehet létrehozni egy áramló elektronok és protonok a légzőkörben: indul az első sor I, a második - a komplex II.
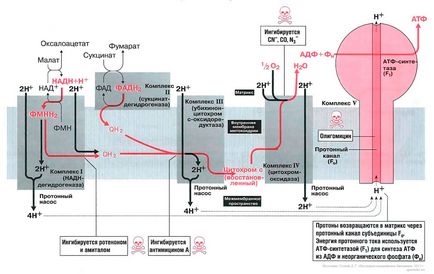
Komplex I [szabály]
Az elektronok áramlását a NADH kezdődik. Energia a szintézis ATP annak köszönhető, hogy töltés szeparáció a komplex I, ami a mozgását elektronok (elektromos áram) és a protonok (proton áram). Molekuláris szivattyú komplex I szivattyúk ki négy protonok intermembránján térben. Egyéb komplexek (III és VI) is pumpált protonok intermembrán térben, és elektrokémiai gradiense protonok van kialakítva; végül az összes Ezek a protonok keresztül visszajuttatjuk a proton csatornán ATP szintáz (cm. alább). A komplex I elektronok átkerülnek a NADH ubikinon (koenzim Q). Két elektronok és két proton csökken ubikinon a ubiquinol (QH2), és ubiquinol mozog a membrán vastagsága a komplex III.
Komplex II [szabály]
Az áramlás indul FADN2 protonok. Komplex II tartalmaz FAD protézis csoport több dehidrogenázok (például, szukcinát). Ez FAD csökken FADN2. Továbbá, komplex II transzferek elektronok ubikinon (Q) az ezt követő elektronok átvitelét a komplex III. Jegyezzük meg, a komplex II nem szivattyúzás protonok.
Komplex III [szabály]
A szerepe a elektrondonor jár ubiquinol QH2, amely azután oxidáljuk ubikinon Q és ebben a formában mehet vissza, és a következő pár elektronok és a protonok. Ubiquinol transzferek elektronokat citokróm, amely szállítja őket, hogy komplex IV. A proton pumpa komplex III tekercs 4 protonok a intermembrán térben.
Komplex IV [szabály]
Az elektronok kapott citokróm c, átvisszük az oxigén, és az oxigént teljesen redukáljuk vizet. Komplex IV bocsát ki intermembrán tér csak 2 proton.
ATP szintáz (komplex V) [szabály]
Ez a készlet tartalmaz a „lábak gomba” - alegység F0, amely egy proton csatornát és a „konvex rész” - ATP szintáz (vagy F1). F0 alegység kapta a nevét, mert gátolja oligomicin, alegysége az F1 volt az első felfedezése és izolálása „frakció” között valamennyi elemét a légzési lánc. Proton fluxus áthalad a proton csatornán, és elindít egy molekuláris motort, ami az ADP és Pi reagálnak egymással alkotnak ATP molekulákat.
Szintetizálni egy molekula ATP és szállítsa a citoszolban 4 proton szükséges. A oxidációja egy molekula NADH szabadul + 10 protonok, amelynek energiája elegendő ahhoz, hogy alkotnak 2,5 ATP molekulákat. A oxidációja 1 molekula FADN2 6 protonok megjelent, az energia, ami elegendő az ATP szintézis 1,5 [1].
Szivárgás elektronok képződéséhez vezet a reaktív oxigénfajták [idézet]
Körülbelül 2% az elektronok kiszabadulnak a légzési lánc, és közvetlenül kötődik az oxigénnel, alkotó reaktív oxigénfajták (ROS). Ha a munka sérül légzési lánc, ROS a nagy mennyiségben gyártott. Ezek az anyagok károsíthatják a mitokondrium, ami a növekvő megsértése a légzési lánc. Egy ördögi kör, és az eredmény a felhalmozási különböző elváltozások hatására ROS sejtöregedés bekövetkezik.
Légzőszervi mérgek [idézet]
Olyan anyagok, amelyek gátolják az ATP, potenciálisan toxikus a szervezetre.
Amobarbital és rotenon blokkolja szállítására elektronok a komplex I. rotenon izolált növényi gyökerek Derris (Derris scandens), és gyakran használják, mint egy természetes peszticid. Ő toxicitása alacsony embereknek, nehezen szívódik fel a gyomor-bél traktusban. Azonban, rotenon mérgező a halakra, mint gyorsan felszívódik a kopoltyúk. Ezen túlmenően, a hosszú távú kitettség rotenone veszélyes az emberre, mert ilyenkor a fejlesztés a Parkinson-kór.
Antimicin blokkok szállítására elektronok a komplex III.
Cianid (CN-). a szén-monoxid (CO) és azidok (N3) gátolják komplex IV. Ezért, amikor cianidmérgezés blokkolt aerob anyagcsere-folyamatok, annak ellenére, hogy elegendő oxigénnel a vér. Mivel a megálló az aerob anyagcsere, vénás vért vesz a színe az artériás vér. Továbbá van hyperventilatio, mert köszönhetően a tejsav felhalmozódása serkenti a légúti központ.
Oligomicin blokkolja a proton csatorna (F0 komplex V), és nem ad protonok vissza a mátrixba. Ezért, az ATP-szintáz (F1) elveszti a képességét, hogy szintetizálni ATP.
Bioszintézise ATP oxidatív foszforiláció (Part II) [szabály]
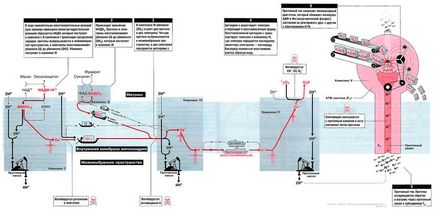
Ábra. 13.1 ábra az elektronok áramlását, és protonok a légzési láncban. Az elektronok és a protonok a NADH + I révén összetett és a FADN2 keresztül továbbított komplex II komplex III. elektronok szállítják komplex IV majd. ahol azok kapcsolódnak az oxigénhez. Ebben az időben, a protonpumpa protonok szivattyúzott a mátrixból a intermembrán tér és visszatért a mátrixhoz a proton csatornán F0-alegységének ATP szintáz (komplex V). Az áramlás a protonok (proton áram) tartalmaz molekuláris motor - F1-ATP-szintáz-alegység komplex. és van egy molekula ADP és Pi oly módon, hogy azokat elegyítjük molekula ATP.
[Citation]
- ↑ A hazai biokémiai kézikönyvekben azonosnak feltételezzük ezek az értékek a „3” és „2”, illetve, azaz oxidációjának 1 molekula képződött NADH három molekula ATP, és az oxidációs FADN2 - 2 ATP-molekula, amely tükrözi az elméleti maximális ATP-szintézis.