Kémiai akció az elektromos áram - studopediya
Sóinak oldatai és savak vízben vagy bármely más oldószer, áramvezetésre, és az úgynevezett elektrolitok, vagy vezetékek a második fajta, szemben a fémes vezetők, a vezetékek első fajta említett.
Az elektromos áram haladhat át táptalajt, melynek villamosan
töltött részecskék, amelyek képesek mozogni.
Amikor az oldott sókat és savat vízben vagy bármely más oldószer (. Etil-alkohol, benzin, benzol, stb) a molekulák két részre oszlik, az úgynevezett ionok, ahol az egyik rész egy pozitív töltés, és a másik - negatív töltés.
Ha egy edényben két fémlap elektrolit szállított úgynevezett elektródák, amelyek által huzal vezet csatlakozik
DC áramforrás, mivel a potenciális különbség az elektródák között az elektroliton keresztül, hogy áram.
Áramátmenettel az elektroliton keresztül kíséri kémiai folyamatot nevezzük elektrolízis. Található elektrolit ionokat vonz a elektródák, mozgó ellentétes irányban, a pozitív ionok - a katód, míg a negatív ionok - az anód.
Közeledve a katód, pozitív ionok belőle előállított a hiányzó elektronok, és azok képezik elektromosan semleges atomok. Az anódon a fordított folyamat játszódik le: anód negatív ionok, így a felesleges elektronokat.
Az átfolyó villamos áram az elektroliton keresztül az elektródákhoz van allokálva egy bizonyos mennyiségű anyagok egy kémiai vegyület az elektrolitban.
A függőség a kiválasztott anyag egy aktuális készlet
Faraday két jogszabályt.
Az első törvénye Faraday az alábbiak szerint történik: az összeg anyag alakult át az elektródok, amikor az aktuális áthalad az elektrolit közvetlenül arányos a villamos energia mennyisége áthaladt az elektrolit.
A folyosón villamos pendant az elektrolitból van allokálva egy bizonyos mennyiségű tömegét olyan anyag, amely az úgynevezett elektrokémiai egyenértékű anyag.
A gyakorlatban számítások meghatározása villamos energia mennyisége nem kényelmes a használata medálok, és amper-óra (Ah).
Mivel az egyik medál egyenlő amper-másodperc között amperóra és függesztett következő összefüggés áll fenn: 1 Ah = 3600 A = 3600-c Cl.
Elektrokémiai ekvivalens K grammban kifejezve, amelyek ugyanahhoz a amperóra villamos mennyiség (g / A * h) T. E. mennyisége anyagok tömege felszabadul az elektrolit és a grammban kifejezve, miközben áthalad az elektrolit egy amper-óra villamos energia mennyiségének .
A második Faraday-törvény kimondja, hogy: ha az azonos mennyiségű villamos energia áramlik át a különböző elektrolitok, tömeges anyagok száma kivált az elektródákon, arányosak a kémiai ekvivalens.
Összehasonlítása alapján az 1. és a 2. Faraday törvény ez azt jelenti, hogy az elektrokémiai ekvivalens arányosak a kémiai ekvivalensei, t. E.
K1 / K2 = a1 / a2 = K3 / a3 =.
Ezért az arányt az elektrokémiai ekvivalens kémiai ekvivalens állandó és egyenlő a
R / a = 3,72 / 0,0372 = 100;
Így a második Faraday-törvény a következőképpen fejezhető ki.
K és X = 0,0372;
Elektrolízis már széles körben használják a különböző iparágakban: A galvanoplasztikai, galvanizálás, tisztítására (finomítására) és más fémek.
galvánelemek
A vezetékek első fajta (szilárd) és a második típusú (folyékony elektrolitok) együtt alkalmaztuk a galvanikus elemek szolgáló egyenáramú források.
A galvánelemek működésük során van egy az ionok mozgását és lerakódás az elektródákon az elem, kibocsátott az elektrolit anyagot.
A legegyszerűbb elem galván réz-cink.
Into egy üvegedényt oldattal töltött kénsav vízben, merített réz és cink lemezek, amelyek pozitív és negatív pólusa az elem.
Amikor az áramkör zárása elem bármely vezetőn belül ez az elem át folyó áram a cink negatív lemez a pozitív réz, és a külső áramkör réz cink.
Hatása alatt a jelenlegi a sejten belül pozitív hidrogénionok mozognak az irányt a jelenlegi, a negatív ionok-maradék - az ellenkező irányba.
Érintkezik egy vörösréz lemez, pozitív ionok hidrogén ad ez a díjakat, és a hidrogén-gáz buborékok halmozódik a felületén.
Ugyanakkor, a negatív ionok a kénsav maradékot adják díjak cinklemezt. Tehát van egy folyamatos töltést lemeztag, amely támogatja a potenciális különbség (feszültség) annak terminálok.
Izolálása hidrogén a réz lemez tag gyengíti az intézkedés - polarizáló elem.
A jelenség a polarizáció, hogy felhalmozódnak a pozitív elektród generál hidrogén-kombinációban további fém elektród potenciál különbséget hívjuk elektromotoros erőt polarizáció. Ez elektromotoros erő ellentétes irányú elektromotoros erő sejt.
Továbbá, a hidrogén buborékok, hogy fedezze része a rézlemez, csökkenti annak hatású felületet, és ez növeli a belső ellenállása a cella.
Polarizációs venni az elemek olyan nagy, ami alkalmatlanná teszi gyakorlati célokra.
Annak érdekében, hogy megszüntesse a jelenség a polarizációs abszorber vezetünk az elem (depolarizátor), amely úgy van kialakítva, hogy megköti a hidrogén és annak nedopuskaet felhalmozódása eleme a pozitív pólushoz.
Depolarizers lehet vegyi anyagok, oxigén-dús vagy klór.
Elektromotoros erő egy réz-cink elem 1.1V, és a belső ellenállás függvényében üzemidő - 5.10 Ohm.
A szén-cink cellákból pozitív pólus lemez szén,
és negatív - cink rúd.
Depolarizátor ezen elem alatt préseljük nagynyomású keverék nevezett agglomerátum. Ez egy peroxidot a mangán és a grafit.
Az elektrolit a szén-cink cellát használunk vizes ammónium-klorid.
A elektromotoros ereje cink-szén sejt 1,4-1,5 elején kisülésből átlagos értéke 0,9-1,1 V, és a belső ellenállás függvényében a szerkezeti elem - 0,25-0,7 ohm elején mentesítés, és 1,4-5 ohm végén.
Cink-szén elemek termel a hazai ipar úgynevezett száraz cella, csésze típusú és galetnogo nagyon kényelmes szállítására és a közlekedés.
A száraz elemeit csésze-típusú pozitív pólust belsejébe helyezzük az agglomerátum cink dobozban. amely arra szolgál, mint a negatív pólus tagja.
A tér között, a falak, a doboz és a cink agglomerátum tele paszta, amelyek ammónium-klorid és burgonyaliszt oldatot.
Fent összehordott halmozott karton bélés. amely nasyplyut réteg fűrészpor; felső porvédő tömítést.
Ezután öntsük a gyantát tagja, amelybe egy cső van behelyezve. Célja a cső - eltávolítására keletkező gázok az elem belsejében.
A kilépés a szén elektród gyantát nasazhivajut réz kupak
Csavarok és anyák csatlakoztatásához karmester.
Ahhoz, hogy a tetején a cink-box (negatív pólus) van forrasztva szigetelt rugalmas vezetéke. Az a doboz aljára helyezzük a hőszigetelő bélés.
Az ostya sejt egy cink negatív elektródalemez, pozitív - tömörített sós keksz mangán-dioxid por, szén.
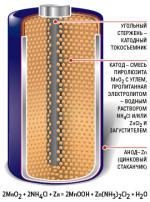
A külső felülete a cink lemez borított grafit réteggel gyanta részecskék vezetőképességét.
A vinil-kloridot alkalmazunk a szigetelő fólia.
Wafer elemek kompakt és azok aktív anyagok (különösen a cink-) használunk jobb, mint a csészében tagja.
Akkumulátor készülék az úgynevezett, képes felhalmozni, és bizonyos ideig még fennmaradhat, elektromos energia kémiai folyamatok.
Az akkumulátor, mint a electroforming sejt, elektromos áram következtében kémiai folyamatok.
De ellentétben az akkumulátort a sejtben keletkező kémiai vegyületek nem bonthatók meg újra, és hozta be a kiindulási állapotban egy külső forrásból áramot.
Ezért galvánelemek nevezzük elsődleges és akkumulátorok - másodlagos vagy visszafordítható.
Ismételt feltöltési és kisütési nem csak káros az akkumulátor, de még javítani annak tulajdonságait, mivel az összes munka mélyebb rétegeibe elektródalapköteget.
Attól függően, hogy a készítmény az elektrolit elemek lehetnek savas és lúgos.
Legegyszerűbb sav akkumulátor
Két Ólomlap (elektród) elmerül a elektrolit, amely a víz, enyhe kénsav hozzáadásával.
Állandó áram külső forrásból, áthaladva az elektrolit bomlik azt alkotórészeire.
Belül a mozgás az elektrolit bekövetkezik H2 pozitív hidrogén ionok a lemezhez csatlakoztatott negatív kapcsa egy áramforrás és negatív oxigén ionok O egy lemezhez csatlakozik a pozitív kapcsa az áramforrás.
Ennek eredményeként a elektrolízis oxidálódik a pozitív elektród ólom és szivacs ólom képződik a negatív elektródán.
Ha az akkumulátort leválasztják a áramforrás és közel van néhány energiát vevő, az akkumulátor áramforrás maga szeretne egy elektrokémiai cella, amelyben az elektródok lemezeket, amelyek különböznek egymástól a kémiai összetétele.
Savas elektrolit elemek, mint fentebb jeleztük, arra szolgál, savas oldat fajsúlya.
- A sűrűsége a megoldás a szám, amely jelzi, hogy hányszor tömege ez a megoldás nagyobb, mint a víz tömege azonos térfogatú.
- Ha oldatot készítünk az akkumulátor, kénsavat öntünk egy vékony sugárban vizet.
- Lehetetlen vizet önteni a kénsav, mivel a gyors fröccsenés történni sav, ami égési sérüléseket okozhat.
- Víz az elektrolitot kell desztillált.
- akkumulátor EMF sűrűségétől függ az elektrolit és nem függ a mérete és névleges kapacitását.
- A folyamat során az akkumulátor töltési és kisütési zlektrolita sűrűsége nem állandó marad, mivel ezeket a változtatásokat az elektromotoros erő és a feszültség egozazhimah.
Menetrend változás feszültség
sav akkumulátor:
1 - egy díj,
2 - a kirakodás során.
A villamos energia mennyisége, hogy az akkumulátor adhat bizonyos kisülési áram a legkisebb megengedett feszültséget, az úgynevezett kapacitását.
Ez megegyezik a termék a kisülési áram amperben, hogy a kisülési időtartamát órában és van kifejezve amper-óra.
Csatlakozó diagram sav akkumulátor lemezeket.
Az akkumulátor kapacitása függ az aktív készítmény, az összeg a jelenlegi és a hőmérséklet.
Alatt a névleges kapacitás, hogy megértsék a villamosenergia-mennyiséget, hogy ad egy teljesen feltöltött akkumulátort
10-órás kisütési módban és a hőmérséklet 25 ° C-on
Így az akkumulátor küld egy névleges kapacitását, kisütés 10 órán sokk számszerűen értékével egyenlő 0,1 a névleges kapacitás.
Növelésével a kisülési áram, az akkumulátor kapacitása csökken, mivel a felület bevont lemezeken ólom-szulfát elektrolit és nehéz hozzáférés a belső réteg az aktív tömeg.
Ahogy a hőmérséklet csökken, a viszkozitása az elektrolit növekszik, ami szintén megnehezíti a hozzáférést a belső rétegek az aktív massza és csökkenti az akkumulátor kapacitása.
Kapacitásának növelése az akkumulátor lemezeket, mint több párhuzamosan kapcsolt.
Mindegyik csoport a pozitív és negatív lemezek működik, mint az egyik nagy tányér, amelynek területe egyenlő a területének összege a csatlakoztatott párhuzamos lemezek.
Mivel a pozitív lemezek között kell lennie a negatív, a számos negatív lemezek mindig eggyel nagyobb, mint a számos pozitív.
Ezen körülmények között a, mindkét oldalán a pozitív lemezek érintkeznek az elektrolittal (amikor a pozitív lemezek oldalú lánc- és a rövidzárlatot előfordulhat érintkezve negatív lemezek).
Helyhez savas akkumulátorok gyártott üveg vagy kerámia edények. Elemek konténerekben fából készült hajók, illetve ólommal bélelt sav-szigetelő anyag.
Savas akkumulátorok használják a villamos szerelési helyhez kötött típusú és autóval.
Mivel a hordozható elemeket használnak túlnyomórészt alkáli elemet.
Az alkáli elemek.
Hajók lezárt alkáli elem vékony acéllemezből és a nikkel a külső oldalon. A központban a tartály fedél van egy kiöntőnyílás elektrolit akkumulátorok.
Eds alkáli elem állapotától függ az aktív tömegének a lemezeket. A hőmérséklet és az elektrolit sűrűség EMF függ enyhén és csak alacsony hőmérsékleten, közel nulla, akkor hirtelen nagymértékben megváltozik.
A feszültség a végén az akkumulátor 1,8 V, a töltés befejeződött - 1,5-1,55 V;
EMF lemerült akkumulátor - 1,3 V.
Az előnye, alkáli elemek, hogy
- nem igényelnek kórházi ápolás;
- Nem fél, hogy rázza;
- lehet hosszú a ritkított állapot;
- vegye ki a rövidzárlat, ami savas akkumulátorok nagyon veszélyes;
- az önálló kisülés a alkáli elem kisebb, mint a sav.
Attól függően, hogy az anyag a elektródok alkáli elemek lehet nikkel-kadmium, vas-nikkel, ezüst-cink, arany-cink és a gáz.
Használata nagy méretű arany-cink elemek korlátozza a magas költségek.
Gáz akkumulátorok egyszerű és olcsó, de a technológia még nem eléggé fejlett a termelés.
A legszélesebb körben használt nikkel-kadmium (KH)
és nikkel-vas (LS) akkumulátorok, amely arra szolgál, mint egy elektrolit oldat, kálium-hidroxid vizes; elektrolit sűrűsége 1.2.
Szerint a adatkezelő eszköz és elektromos akkumulátor és KH LS némileg eltérnek egymástól.
Az aktív masszát préseljük brikett (csomagokat), majd brikett gyűjtöttünk az egyes lemezek.
A Type LS akkumulátor negatív lemezek egy több, mint pozitív.
A KH akkumulátor pozitív lemezeket egy több, mint a negatív.
Az egyik pólus az akkumulátor csatlakoztatva van a hajó (a woh - negatív,
míg az SC - pozitív pólus).
Ezüst-oxid akkumulátor egy műanyag tartály, amelyben vannak elhelyezve a pozitív és negatív elektródák állnak az egyes lemezek.
Negatív elektródákkal készült lemezek cink-oxid, zárt a védő csomagolásban olyan anyagból, amely jól továbbítja az elektrolit, de megtartja a fémes részecskék.
Pozitív lemezek készülnek ezüst.
A készítmény az akkumulátor elektrokémiai cellákat vagy az akkumulátort, számos elemet sorba kötve, azaz a. E.
a katód az első elem van csatlakoztatva az anód a második,
a második katód -, hogy az anód a harmadik, és így tovább ..
És ily módon szabad elektródok, nevezetesen egy anódot és katódot az első tag utolsó rendre pozitív és negatív pólusa az akkumulátort.
Annak megállapítására, elektromotoros erő az akkumulátor az n-savas akkumulátorok vagy elektrokémiai sejtek egyik eleme EMF Eo, és a belső ellenállás Ro = E EMF NE0 akkumulátort, és a belső ellenállása R = NR0.